La ré-oxydation des cofacteurs par fermentation
I. Introduction
Comme cela est dit dans le sous-chapitre 01, la glycolyse produit un certain nombre de cofacteurs réduits, deux par glucose consommé, et qui doivent être ré-oxydés au risque que la glycolyse s’arrête. En effet, la cellule est un espace fini et le stock de cofacteurs oxydés limité.
La cellule doit donc recycler en permanence ses cofacteurs réduits pour maintenir son stock de cofacteurs oxydés.
Le pyruvate, le dernier produit de la glycolyse, est le point de départ de deux stratégies de ré-oxydation des cofacteurs. L’une des stratégies exploite toutes les ressources disponibles dans la cellule, c’est la fermentation. L’autre stratégie nécessite l’apport d’un accepteur final d’électron, c’est la respiration (traitée dans le sous-chapitre 02).
Définition de la fermentation : processus métabolique oxydatif cytoplasmique permettant la ré-oxydation des cofacteurs réduits,accumulés dans la cellule, tout en produisant de l’ATP. La fermentation se fait sans intervention d’un métabolite extérieur : c’est un processus en vase-clos. Le point de départ de la fermentation est quasiment toujours le pyruvate, et peut aboutir à la production de dioxyde de carbone, H2, éthanol, lactate, propionate, acétate et AG à courtes chaînes (produits terminaux de fermentation) … Un seul transporteur d’électron est mobilisé : NAD+/NADH,H+.
Ce processus est très répandu (mais ne veut pas dire fréquent dans le temps) chez les microorganismes, et également très diversifié. Il en reste quelques traces chez les organismes supérieurs, comme la fermentation lactique musculaire.
Chez les microorganismes, la fermentation peut être facultative, comme chez les AAF (aéro-anaérobies facultatifs) ou obligatoire (anaérobies strictes ou anaérobies aérotolérants).
La fermentation n’est pas un processus énergétique !!! C’est une stratégie de ré-oxydation des cofacteurs, en vase-clos !!!
La mise en place de la fermentation se fait généralement dans une situation dramatique pour la cellule : l’absence d’accepteur final…
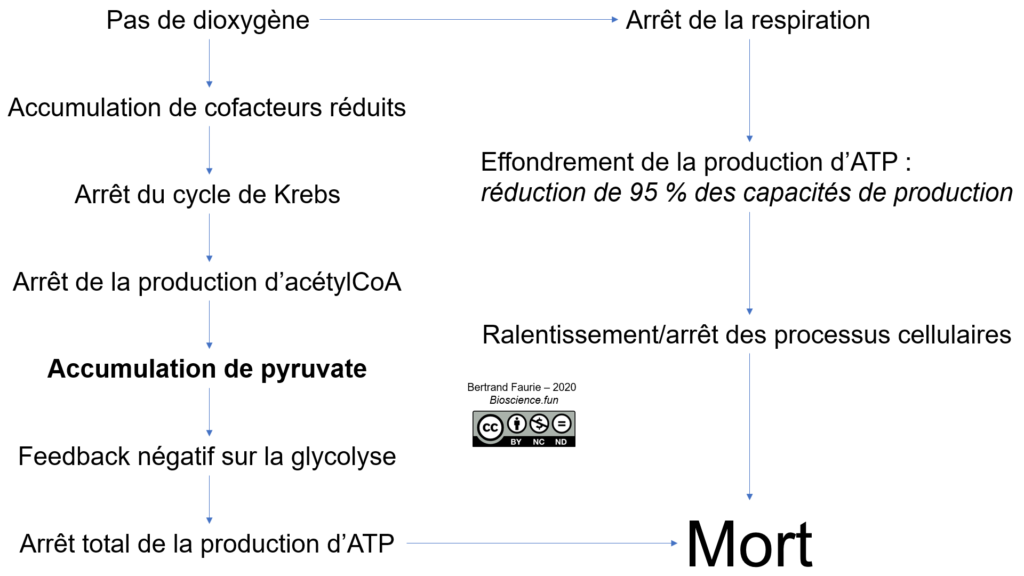
C’est parce que le pyruvate s’accumule sous l’effet de la glycolyse, qu’il va être le meilleur réactif pour tenter de ré-oxyder les cofacteurs (voir figure 0210302)
II. Réalisation des fermentations
II.A.Des substrats particuliers
Les nutriments utilisés par la cellule bactérienne (ou autre microorganisme) doivent pouvoir :
- Dans un premier temps : être oxydés contre un cofacteur qui sera réduits. L’enthalpie libre résultante de cette réaction rédox permettant de générer des liaisons à haut potentiel (anhydride d’acide ou énol-P). Ces liaisons permettront ensuite la phosphorylation au niveau du substrat de l’ADP en ATP (la glycolyse en fait) ;
- Dans un second temps : les produits obtenus devront pouvoir être réduits pour ré-oxyder les cofacteurs réduits durant la glycolyse.
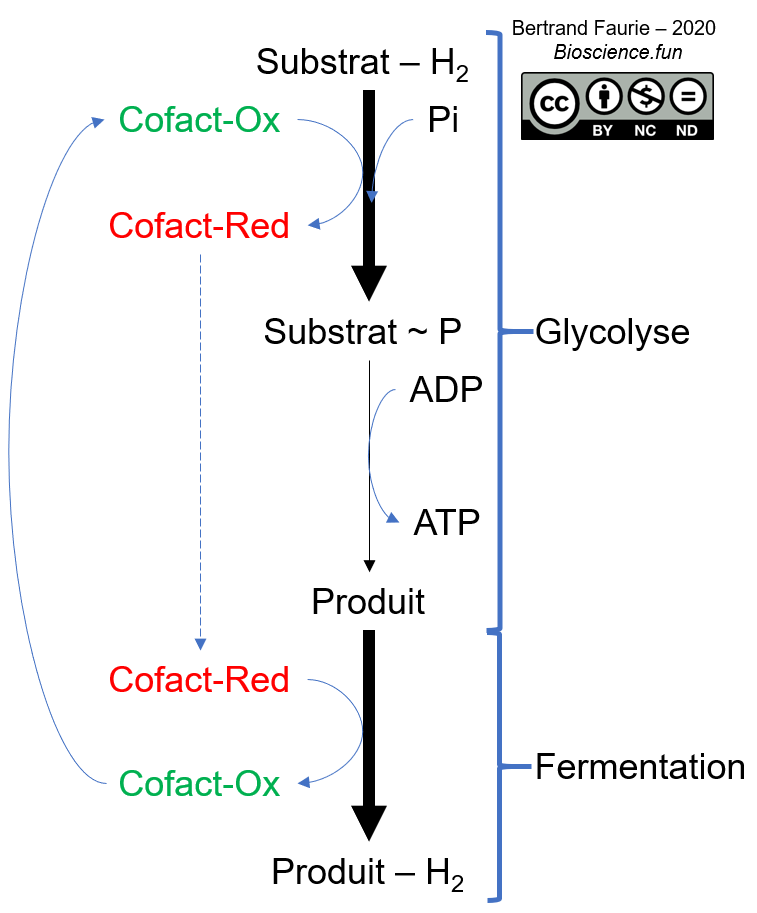
Les oses permettent cette double-réactivité grâce notamment à l’équilibre entre les fonctions aldéhydes/cétones et alcools. Mais d’autres substrats en sont capables, comme les acides organiques (malate, citrate, …) ou les acides aminés (Ala, Gly, Arg, …).
II.B.Diversité des fermentations
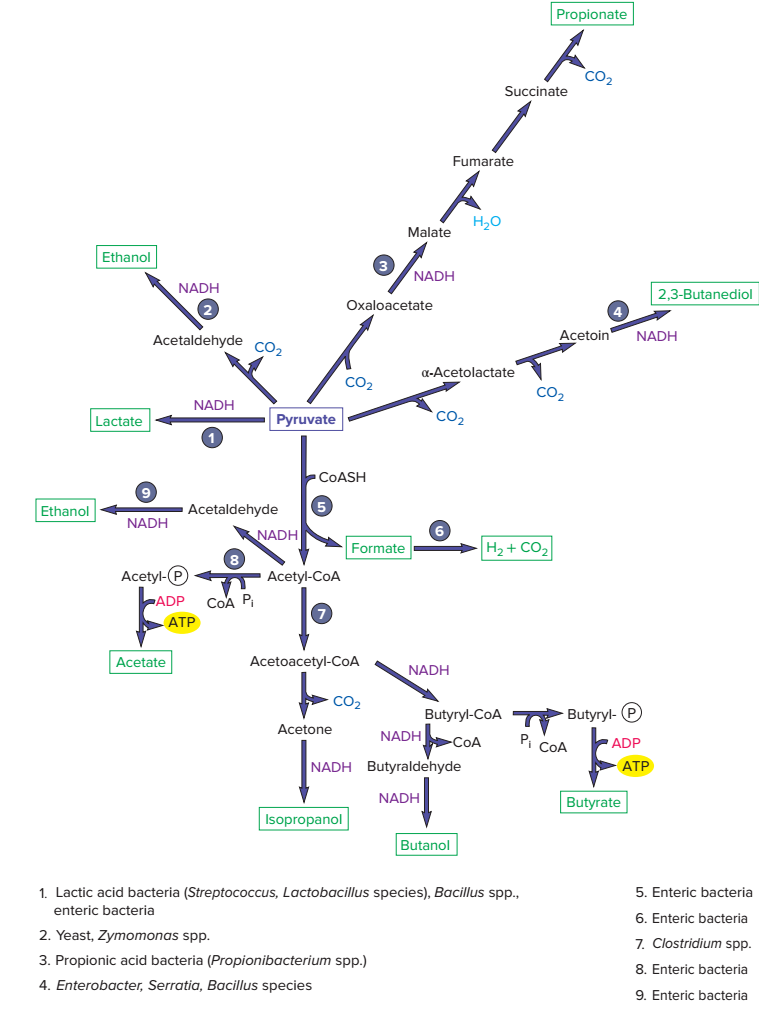
Chez les bactéries, on peut trouver voir (document 0210202) :
- La fermentation homolactique : le seul produit formé est le lactate, directement à partir du pyruvate ;
- La fermentation hétérolactique : formation de lactate, mais également d’acétate, d’éthanol et de CO2 (gaz) ;
- Fermentation des acides mixtes : lactate, acétate, succinate, éthanol, acide méthanoïque (test RM positif). Fiche technique ;
- Fermentation butanediol : fermentation acides mixtes + production d’acétoïne et butanediol (test VP positif). Voir fiche technique précédente.
Chez les levures, on observe essentiellement la fermentation alcoolique, avec production d’éthanol et de CO2 (gaz).
II.B.La fermentation lactique
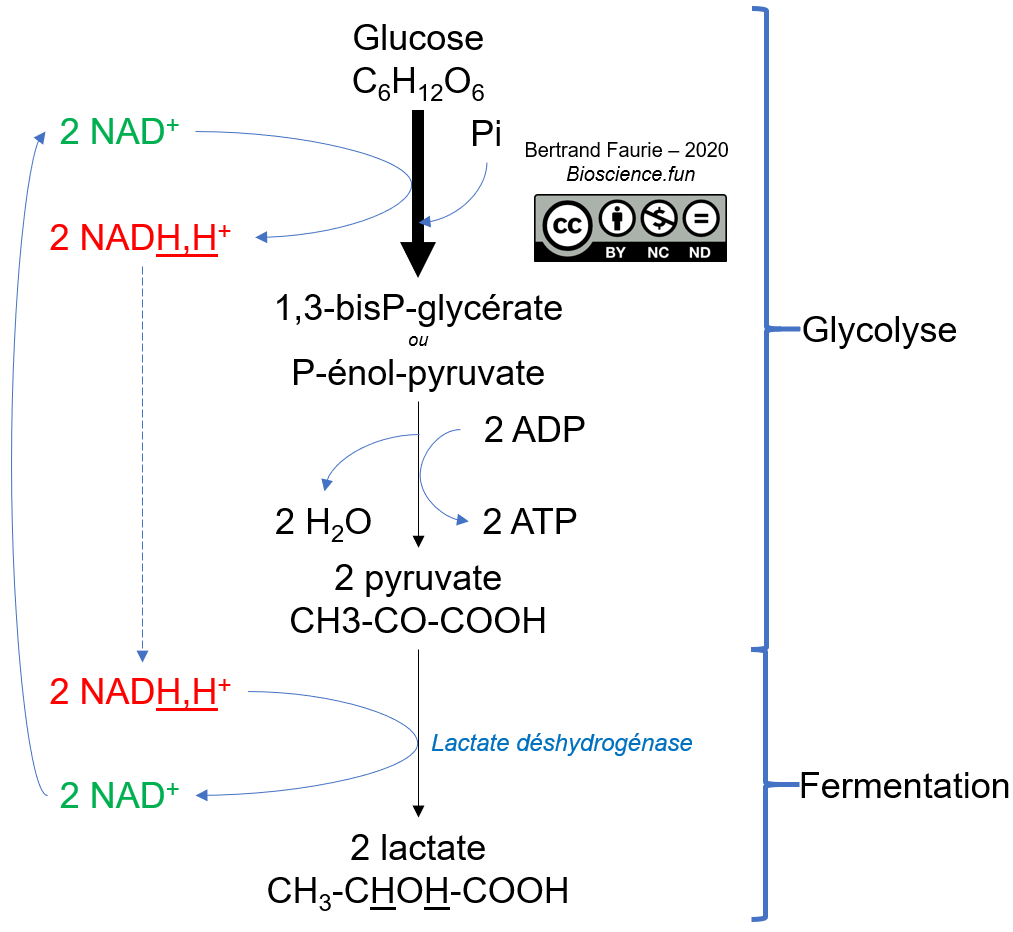
Au final, la fermentation homolactique permet la production de deux ATP par glucose, soit -60 kJ/mol. A titre de comparaison, la respiration permet une libération d’énergie de -2000 kJ/mol. La réaction de fermentation lactique, depuis le glucose, présente un ΔGR0’ de -200 kJ/mol.
Biotechnologies issues de la fermentation homolactique
LE YAOURT
L’acide lactique est obtenu par fermentation opérée par les bactéries lactiques lors de la fabrication du yaourt et autres laits fermentés …
La dénomination «Yaourt» est réservée au lait fermenté obtenu, selon les usages loyaux et constants, par le développement des seules bactéries lactiques thermophiles spécifiques dites Lactobacillus bulgaricus et Streptococcus thermophilus qui doivent être ensemencées simultanément et se trouver vivantes dans le produit fini à raison d’au moins 10 millions de bactéries par gramme de yaourt.
Le lait livré à l’usine est plus ou moins écrémé pour faire, selon les cas, des yaourts maigres, des yaourts au lait entier. On ajoute de la poudre de lait ou du lait concentré pour donner au yaourt une consistance plus ferme. La pasteurisation à 92°C détruit des germes pathogènes. On refroidit à 45°C, température idéale pour la vie des bactéries. Le lait ensemencé, éventuellement additionné de sucre ou d’arômes naturels, est versé dans les pots de yaourts. Les pots sont fermés et mis en étuve à une température de 43°C à 45°C pendant 2 à 3 heures pour fermentation.
Les bactéries se reproduisent par millions et transforment alors une partie du lactose contenu dans le lait en acide lactique. Cette transformation s’appelle la fermentation lactique. La production d’acide lactique acidifie le lait, ce qui entraîne la coagulation de la caséine du lait et le développement des arômes. Les pots sont ensuite refroidis entre 2°et 4°C
La fermentation lactique est l’étape décisive assurant la transformation du lait liquide en un gel. Les deux bactéries lactiques employées, Streptococcus thermophilus et Lactobacillus delbrueckii subsp. bulgaricus ont été initialement retenues pour des raisons historiques, parce que fréquemment trouvées dans les laits fermentés traditionnels du Moyen-Orient. Mais il y a de bonnes raisons de continuer à les utiliser, car les deux espèces interagissent en synergie.
En début de fermentation, les S.thermophilus se développent rapidement. Ils absorbent le lactose et le transforment en L(+) acide lactique, ce qui provoque une baisse du pH (acidification). Ils amorcent aussi le développement de la population de Lb. bulgaricus en produisant des composants capables de stimuler leur croissance, comme l’acide formique et le gaz carbonique.
En retour, Lb. bulgaricus hydrolyse la caséine grâce à une protéinase fixée sur ses parois, qui après d’autres réactions enzymatiques donnent des acides aminés (en particulier la valine). Ces composés indispensables à la croissance des bactéries ne sont pas en quantités suffisantes dans le lait en début de fermentation. S. thermophilus qui a une activité protéinase plus faible bénéficie donc de la présence du lactobacille.
Grâce à cette action conjointe les deux espèces croissent rapidement et métabolisent suffisamment de lactose en acide lactique pour que la fermentant soit terminée en 3 à 4 heures, là où chacune auraient dû passer seule 12 à16 heures pour obtenir la même acidité.
Ces deux espèces bactériennes synthétisent aussi des polysaccharides qu’elles excrètent à l’extérieur de la cellule (nommés exopolysaccharides). Ce sont des polymères de galactose, glucose et rhamnose, produits en quantité variable suivant les souches. La présence de ces composés est très recherchée car ils augmentent la viscosité du yaourt et donnent une sensation d’onctuosité au produit, appréciée des consommateurs.
Les souches bactériennes produisant le plus d’exo-polysaccharides ont été sélectionnées afin de se dispenser d’ajouter des épaississants et gélifiants au produit.
Le lait est une émulsion formée par un mélange aqueux de lactosérum, dans lequel sont dispersés des micelles de caséine et des globules gras. La micelle de caséine est un agrégat sphérique (de 120 nm en moyenne) qui est constituée de 10 à 100 sous-micelles reliées entre elles par des ponts phospho-calciques. Elle est très hydratée. L’eau est fixée au chevelu micellaire sous la forme d’une couche d’hydratation en surface. Les micelles de caséine portent initialement une charge négative nette (quand le lait est encore au pH 6,7).
La précipitation de la caséine résulte de l’abaissement du pH lié à la formation d’acide lactique par les bactéries lactiques. L’acide lactique porte des charges positives qui neutralisent les charges négatives des colloïdes. À pH 4,6 les charges positives et négatives s’équilibrent. C’est ce qu’on appelle e point iso électrique de la caséine. La neutralisation des charges de surface permet aux micelles de se rapprocher (pour un pH de 5,8-5,5) puis de s’agréger par des liaisons électrostatiques et hydrophobes (dès un pH de 5,2).La solubilisation du calcium est totale à pH 5,0 suivie par une gélification totale à pH 4,9.
LA CHOUCROUTE
Principe de fabrication de la choucroute. L’ajout de sel permet d’inhiber la croissance de certains microorganismes défavorables (bactéries GRAM négatives) au profit des bactéries lactiques (le sel est un conservateur). Durant la phase de déshydratation, la fermentation homolactique se produit.
Les principales bactéries responsables de la fermentation de la choucroute sont : Leuconostoc mesenteroïdes (coque GRAM +) et Lactobacillus plantarum (bacille GRAM +). Leuconostoc cesse son activité pour 1 % d’acide lactique dans le produit. Les lactobacilles poursuivent jusqu’à pH = 1.6.
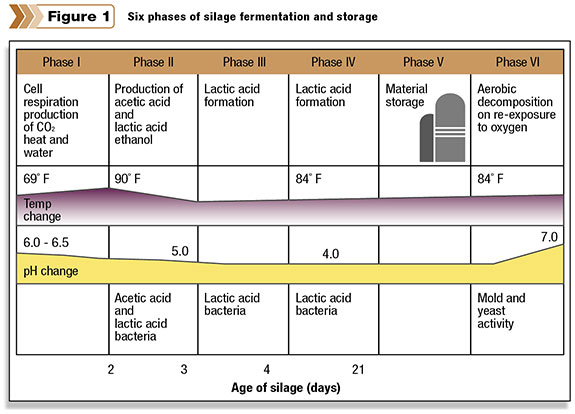
LA CONSERVATION DU FOURRAGE
Le fourrage est conservé grâce à l’action de microorganismes homo/hétérolactiques comme Lactobacillus spp. La fermentation du fourrage permet de limiter la croissance de Clostridium qui provoque la putréfaction de la ressource, qui devient alors inutilisable. L’abaissement du pH permet également de limiter la croissance de Listeria monocytogenes, dont les toxines peuvent provoquer des avortements spontanés chez les animaux, ou une la mortinatalité accrue.
La fermentation du fourrage est maintenue dans des conditions anaérobies par stockage du foin sous une bâche hermétique ou dans un sachet (balles de foin).
II.C.La fermentation alcoolique
Bien que la production d’éthanol par fermentation soit possible chez les bactéries, il n’y a que les levures (Eucaryotes) qui sont capables de produire directement de l’éthanol à partir de pyruvate.
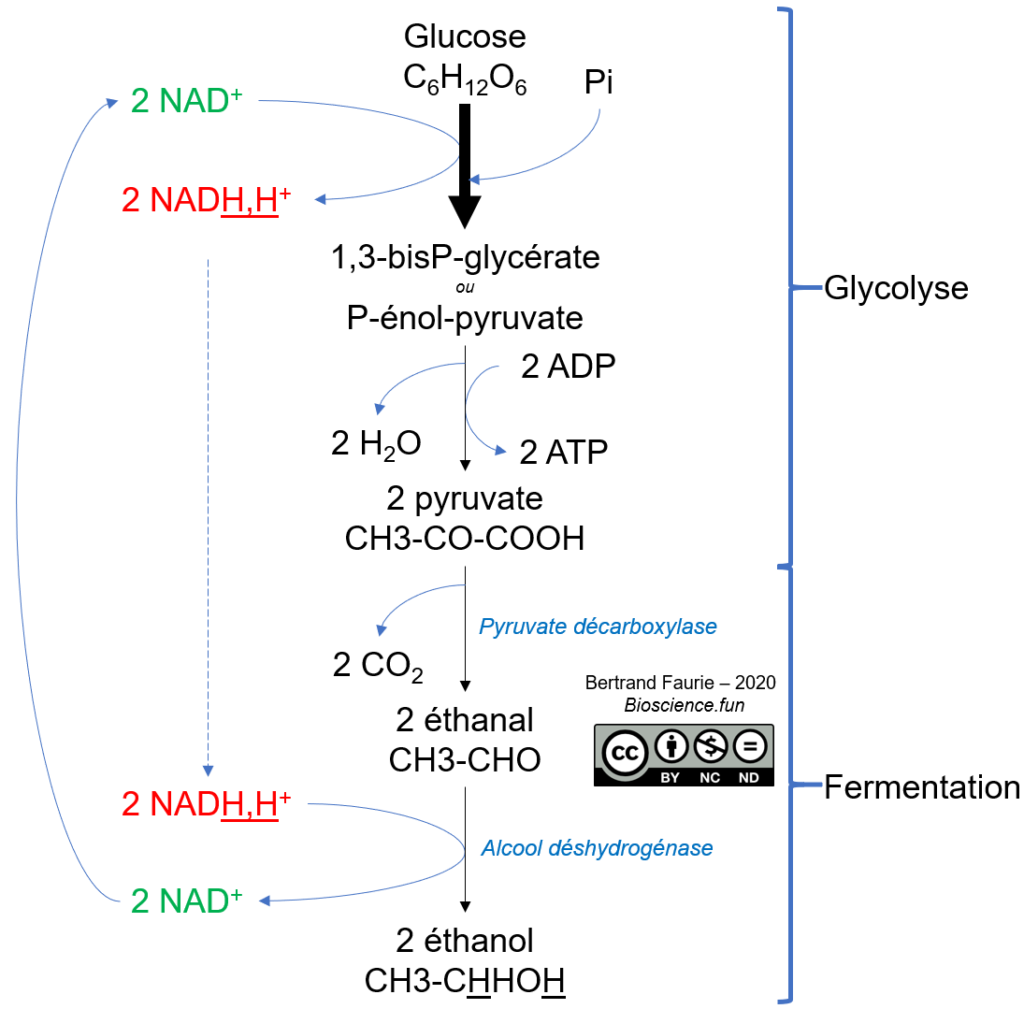
Au final, la fermentation alcoolique permet la production de deux ATP par glucose, soit -60 kJ/mol. La réaction de fermentation lactique, depuis le glucose, présente un ΔGR0’ de -240 kJ/mol.
Biotechnologies issues de la fermentation alcoolique
Fabrication de la bière
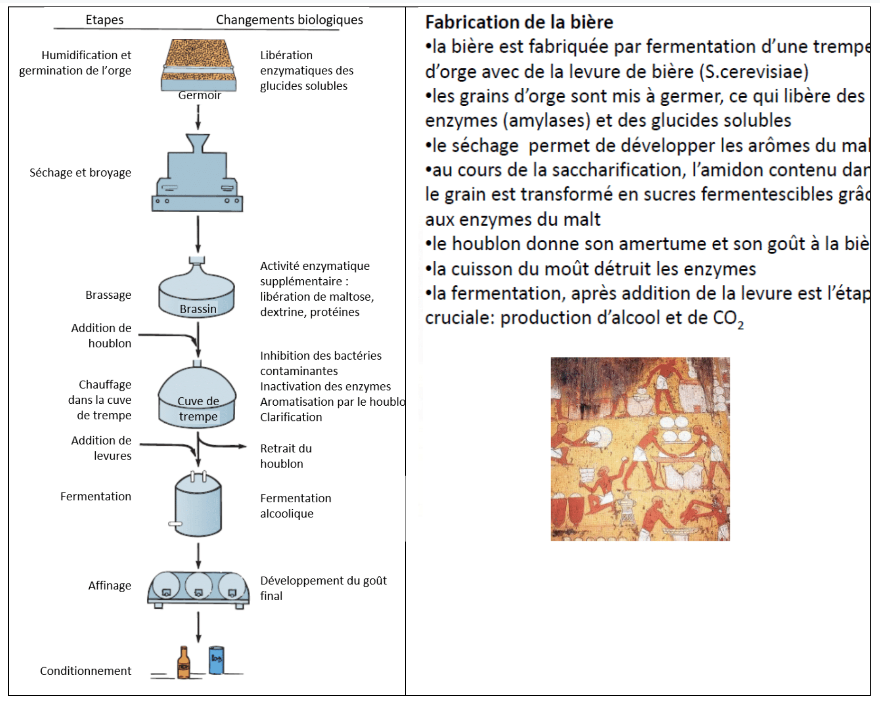
Fabrication du pain

Fabrication du vin
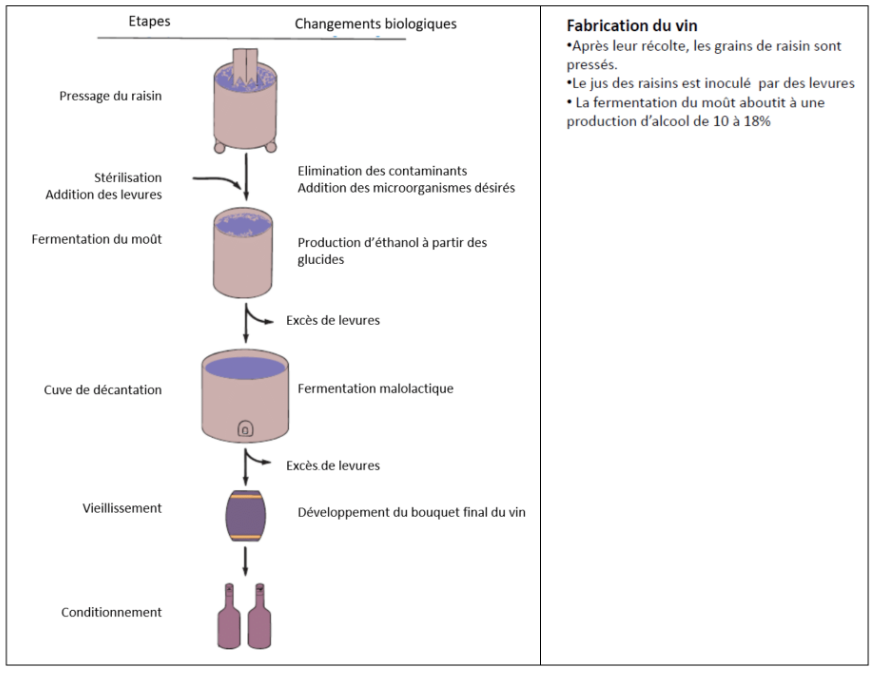
III. Effet Crabtree
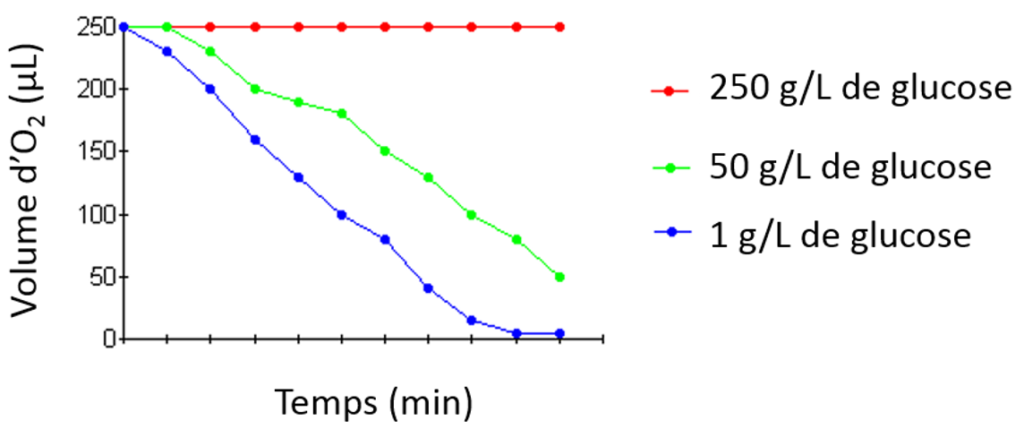
L’effet Crabtree, découvert par Crabtree en 1929, est un cas particulier d’apparition de la fermentation. L’observation a été faite lors de l’étude de la consommation de glucose par des cellules cancéreuses.
Dans ce cas, malgré une grande richesse en substrat carboné, ET la présence d’un accepteur final des électrons, les cellules arrêtent de respirer et se mettent à fermenter. Sous effet Crabtree, les gènes codant les protéines de la chaîne respiratoire sont réprimés. Toutes les souches ne sont pas « Crabtree + », mais ce phénotype peut être induit notamment par des facteurs de transcription proches de Gal4 (impliqué lui dans le métabolisme du galactose). Il y aurait alors une forte stimulation de la glycolyse et un afflux de glucose dans la cellule.
Cet effet est mal compris à l’heure actuelle et pose de sérieux problèmes dans les processus biotechnologiques. Il existe plusieurs hypothèses pour l’expliquer que sous l’effet d’une forte concentration en glucose, les cellules préfèrent fermenter :
- Limiter un épuisement rapide des ressources de l’environnement et l’accumulation de déchet (forte variation de pH) ;
- Limiter l’apparition d’une compétition pour le NAD et le Pi au profit de la glycolyse, ce qui provoquerait un arrêt des autres voies métaboliques ;
- Empêcher un emballement métabolique : la respiration libère beaucoup de chaleur, ce qui augmente encore la vitesse des réactions, …
